第579号 バリデーション(適格性評価)時の現場でのリスクアセスメントについて
現場でも正確にリスクを特定し、分析し、評価する必要がある?
> ご存知のように改正GMP省令においては、製造業者等は品質リスクマネジメントを活用して、PQS(医薬品品質システム)を構築し、医薬品に係る製品について、製造所における製造管理及び品質管理を行う必要があるとなっています。
■ 改正GMP省令の第3条の4 品質リスクマネジメントでの要求事項

※ このように、現場においても品質リスクマネジメントが重要視されていることが、お問い合わせに繋がっていると考えます。
設備・装置のリスクマネジメントとはどうしたら良いの!
> 当社内でも、このような会話を時折耳にします。
このようなときには、ひとつの考え方として、次のようなフロー等の概要から理解しています。
□ ICH(日米 EU 医薬品規制調和会議)やISO31000では、設備または施設の設計時・据付時・運用時、そして設備・施設の廃棄までライフサイクルを通して品質リスクアセスメント活動を行い、必要に応じてリスクを低減させる対策を講じることを推奨しています。
その中では、以下のようなリスクマネジメントプロセスフローを確認することが出来ます。
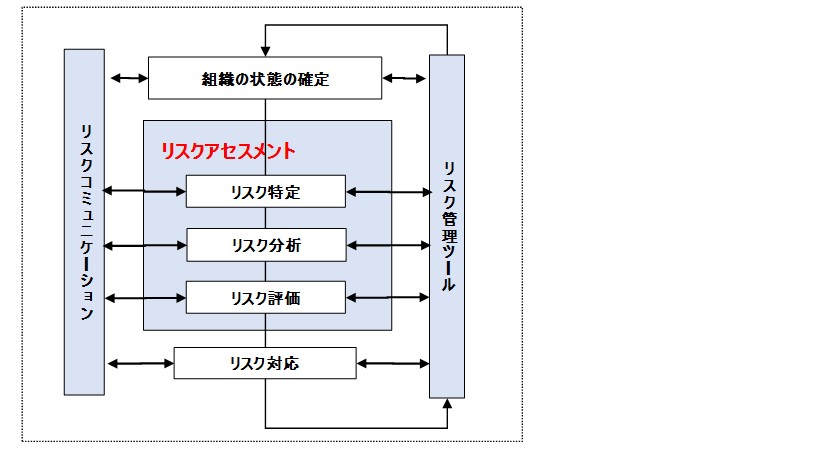
このようにリスクアセスメントは、リスクをどのようにコントロールするかについて判断をするため、品質リスクマネジメントプロセスの中で最も重要な段階であり、正確にリスクを特定し、分析し、評価する必要があると言われています。
次に、リスクアセスメントについて経済産業省の資料から概要をご紹介したいと思います。
リスクアセスメントは品質マネジメントで最も重要な段階!!
> ここでは、経済産業省/国立研究開発法人日本医療研究開発機構の資料に、当社が少し手を加えたものをご紹介します。
【リスクアセスメントの視点】

※ 当社も、上記の各視点などで、リスクを特定・分析・評価し、リスク対応出来る様に、バリデーション(適格性評価)の実施仕様をお客様とご相談しながら決定するようにしています。


※ 当社は、フィールドでバリデーション・キャリブレーションを実施する立場から、規格の要求内容や定義を具体化(具現化)して、お客様に満足して頂ける作業をお届けする努力を続けています。
最後まで、お読みいただき有難うございました。
